编者按:乳腺癌辅助治疗方案众多,引起各系统的毒副作用表现不一,比如化疗药物的腺毒性导致的泪液阻塞、干眼症,是临床中并不少见而又不够重视的不良反应。近日,《乳腺》(The Breast)杂志在线刊载了一项来自中国医科大学附属第一医院金锋教授团队的研究,探讨了乳腺癌辅助治疗中的干眼症患病率及其与治疗间的关系。

乳腺癌辅助治疗的个体化升阶治疗、靶向治疗和其他综合治疗手段进展,改善了患者的远期预后,也存在毒性累积和副作用增多的客观现实。其中,乳腺癌辅助治疗患者的眼毒性,特别是干眼症的临床反映和重视不足引起了笔者的兴趣。
抗肿瘤细胞毒药物和靶向治疗药物对眼部的负面影响已有一些文献报道。尽管分子机制尚不清晰,作为早期乳腺癌中第一个标准治疗方案“CMF”的成员药物,至少25%接受5-氟尿嘧啶治疗的患者有泪溢表现,提示了泪液引流通道固有的脆弱性。Kalra等报告了环磷酰胺和蒽环类药物联合使用引起的泪溢,环磷酰胺也是引起反射性泪溢的可疑药物。紫杉烷类被多次报道诱发泪溢和眼小管狭窄,研究者发现接受多西他赛化疗的患者泪液中含有多西紫杉醇,被认为是引发泪小管炎和泪液引流阻塞的潜在因素。这些研究可能提示,随着细胞毒药物的体内累积,会引发泪液引流通道阻塞,增加了毒性物质与角膜的接触时间从而导致干眼症的发生。
对于实体肿瘤的分子靶向药物的眼毒性较细胞毒药物应更加谨慎,临床医生可能面临更多出乎意料的眼毒性或其他副作用。而仅有为数不多的临床试验将眼毒性纳入研究。其中均报道过曲妥珠单抗联合多替他赛(DH)方案中至少20%患者出现流泪增多的症状,2.4%的患者出现严重结膜炎。美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)签发的曲妥珠单抗标签中提示其眼部副作用包括“常见的干眼症和流泪增加,不明乳头水肿和视网膜出血”,帕妥珠单抗和贝伐珠单抗均标注有“常见的流泪障碍”的副作用,拉帕替尼未报告眼部不良事件。Huillard等回顾重大临床试验和药物标签发现,二者所报告的眼部副作用的发生率和严重程度存在较大差异,临床试验的研究者对靶向药物的眼毒性可能存在忽视和报道不足。
干眼症是眼表的一种多因素疾病,特征为眼泪膜稳态丧失,伴有眼部刺激症状。由于干眼病临床评估结果的差异性,目前没有单一的确定性测试或诊断干眼病的标准达成共识,临床医生对干眼的评估通常基于有效的临床调查问卷结果。
本团队设计了一项旨在探讨乳腺癌辅助治疗患者中干眼症的患病率,及其与治疗间关系的横断面研究。研究共入组423人,暴露组纳入临床诊断为乳腺癌、已接受两周期及以上的辅助治疗或新辅助治疗(包括单纯化疗、单纯靶向治疗或联合靶向治疗)的患者,对照组纳入同时期人口资料匹配的女性。排除标准为:有内分泌治疗史,干燥综合征,近期眼部感染,眼科手术或外伤史,过去一个月内睑缘和眶周皮肤病史或过敏史,急性炎症,带状疱疹感染,其他风湿性免疫系统疾病,或处于哺乳期。本研究采用眼表疾病指数(Ocular surface disease index,OSDI)量表得分评估干眼症及其严重程度。
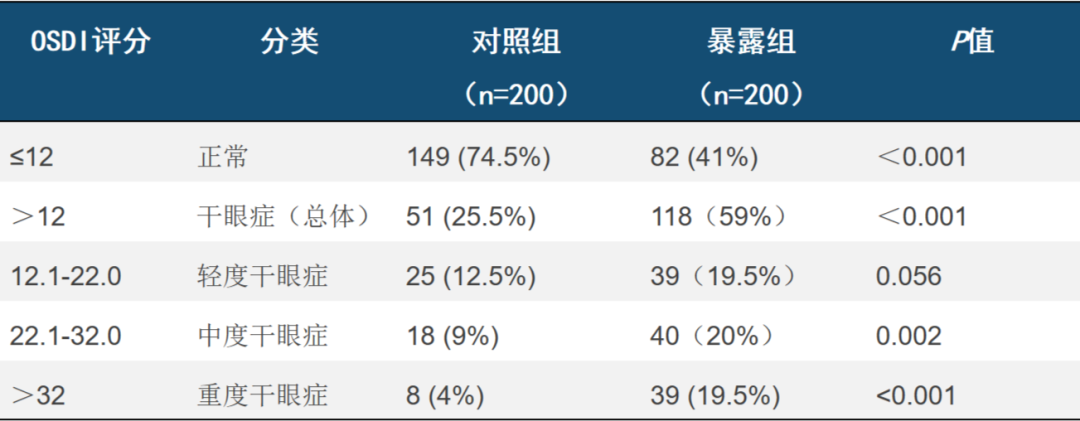
本研究发现接受乳腺癌辅助治疗组干眼症的患病率为59.0%(n=118),明显高于对照组的25.5%(n=51,P<0.001)。其中轻度干眼(OSDI 13-22)高于对照组,但无统计学差异(P=0.056)。中度(OSDI 23-32)和重度干眼(OSDI>32)患病率分别为20.0%和19.5%,明显高于对照组9.0%和4.0%(P=0.002和P<0.001)。
表1. 根据OSDI评分暴露组和对照组的干眼症患病率
对干眼症与临床病理因素的关联性进行分析,发现其与患者Ki-67状态及分子分型显著相关,二者均是决定乳腺癌辅助治疗方案的关键因素。进一步进行干眼症与治疗的单因素分析,发现患者已接受的治疗周期和靶向药物的应用与干眼显著相关(Pearson卡方检验和logistic回归分析,P<0.05)。接受4个周期以上全身治疗的患者,和应用靶向治疗的患者干眼患病率更高(n=66,71.0%;n=47,71.2%)。同时,干眼病的严重程度与已接受的化疗和靶向治疗的周期具有相关性(P<0.01和P=0.01)。手术方案、辅助治疗的时机和密集治疗的应用未发现影响干眼病患病率。
本研究提示对于接受4周期以上化疗或任何靶向治疗的患者,有进行阶段性干眼问卷评估或眼科检查的必要性。
另外,性激素是维持眼表正常生理的重要角色,在各人眼组织(包括泪腺、睑板腺、结膜和角膜等)中已鉴定出雄激素、孕激素和雌激素受体。Gorin MB等和Eisner A等的研究报道,长期作为激素受体阳性乳腺癌标准内分泌治疗的选择性雌激素受体调节剂(SERMs)他莫昔芬,会增加后囊白内障风险并导致视神经乳头水肿等眼毒性。雄激素和雌激素平衡是维持眼表稳态的关键,绝经后女性的雌激素主要来源于肾上腺雄烯二酮和睾酮的转化,芳香化酶抑制剂(AIs)抑制这一外周性转化通路治疗绝经后激素受体阳性乳腺癌,同时也成为引发干眼症的潜在因素,Inglis H和Tolga B在近期分别独立报道了乳腺癌辅助内分泌治疗中,芳香化酶抑制剂会提高干眼的患病风险。
乳腺癌辅助治疗的各个阶段,包括细胞毒化疗、靶向药物治疗和内分泌治疗均有引发干眼症的潜在可能。与普通人群干眼症严重程度的分布不同,乳腺癌辅助治疗患者的干眼症多集中在中、重度水平,并且与已接受的化疗或靶向治疗的周期密切相关。另外,靶向药物为主的辅助治疗是干眼症的显著相关因素。抗癌药物的眼毒性,包括干眼症,在临床上尚没有预防手段。因此,临床医生必须了解此种并发症的可能性,及时干预和治疗干眼症状,从而确保患者辅助治疗的连续、足量和依从。
1. Eiseman AS, Flanagan JC, Brooks AB, Mitchell EP, Pemberton CH. Ocular surface, ocular adnexal, and lacrimal complications associated with the use of systemic 5-Fluorouracil. Ophthal Plast Reconstr Surg 2003;19:216–24. https://doi.org/10.1097/01.IOP.0000066648.33513.3D.2. Kalra R, Chavada B, Madhani NR, Purohit B, Tripathi CB. Cyclophosphamide and/or Anthracyclines Induced Epiphora in Breast Cancer Patients: A Rare Side-effect. Curr Drug Saf 2018;13:62–4. https://doi.org/10.2174/1574886312666170919175614.3. Esmaeli B, Amin S, Valero V, Adinin R, Arbuckle R, Banay R, et al. Prospective study of incidence and severity of epiphora and canalicular stenosis in patients with metastatic breast cancer receiving docetaxel. J Clin Oncol 2006;24:3619–22. https://doi.org/10.1200/JCO.2005.04.4453.4. Esmaeli B, Ahmadi MA, Rivera E, Valero V, Hutto T, Jackson DM, et al. Docetaxel secretion in tears: Association with lacrimal drainage obstruction. Arch Ophthalmol 2002;120:1180–2. https://doi.org/10.1001/archopht.120.9.1180.5. Olivier H, Silvin B, Christine L, et al. Ocular adverse events of molecularly targeted agents approved in solid tumours: A systematic review. Eur J Cancer. 2014 Feb;50(3):638-48. http://doi: 10.1016/j.ejca.2013.10.016.6. Jinfei M, Eric EP, Zihao Z, Feng J. Prevalence of symptomatic dry eye in breast cancer patients undergoing systemic adjuvant treatment: A cross-sectional study. Breast. https://doi.org/10.1016/j.breast.2020.07.009.7. Gorin MB, Day R, Costantino JP, Fisher B, Redmond CK, Wickerham L, et al. Long-term tamoxifen citrate use and potential ocular toxicity. Am J Ophthalmol 1998;125:493–501. https://doi.org/10.1016/s0002-9394(99)80190-1.8. Eisner A, Toomey MD, Falardeau J, Samples JR, Vetto JT. Differential effects of tamoxifen and anastrozole on optic cup size in breast cancer survivors. Breast Cancer Res Treat 2007;106:161–70. https://doi.org/10.1007/s10549-006-9486-3.9. Inglis H, Boyle FM, Friedlander ML, Watson SL. Dry eyes and AIs: If you don’t ask you won’t find out. Breast 2015;24:694–8. https://doi.org/10.1016/j.breast.2015.08.008.10. Tolga B, Goksen II, Aysun SD, et al. The effects of adjuvant hormonotherapy on tear functions in patients with breast cancer. Int Ophthalmol. 2020 Aug;40(8):2077-2083. http://doi: 10.1007/s10792-020-01384-7.
主任医师,教授,博士生导师
中国医科大学附属第一医院乳腺外科主任
辽宁省抗癌协会乳腺癌专业委员会主任委员
中国临床肿瘤学会(CSCO)理事会理事
中华医学会肿瘤分会乳腺肿瘤学组副组长
中国老年学学会乳腺癌分委会副主任委员
北京乳腺病防治学会外科专委会副主任委员
中国抗癌协会乳腺专业委员会常务委员
中华医学会外科分会乳腺癌学组委员
 ?
?





 京公网安备 11010502033352号
京公网安备 11010502033352号