《肿瘤瞭望》:基于BOLERO-2研究,依维莫司早在2012年已经获FDA批准用于治疗ER阳性晚期乳腺癌,国内类似的研究也已接近尾声。从目前的证据,以及您所参加的国内研究初步结果,您如何看待依维莫司在ER阳性晚期乳腺癌中的应用?
邵志敏教授:PI3K/AKT/mTOR信号通路调控异常与肿瘤发生密切相关,依维莫司是口服的mTOR抑制剂,具有抑制肿瘤细胞生长与增殖、抑制肿瘤营养代谢和抗血管生成的作用。2012年,FDA批准依维莫司用于治疗HR+/HER2-绝经后晚期乳腺癌,并获得NCCN等国际指南推荐。该批准主要基于BOLERO-2研究,这项国际多中心3期研究,入组了724例HR+/HER2-绝经后AI进展的患者,结果显示达到主要终点,依维莫司+依西美坦相较于依西美坦无论在研究者评估的PFS(7.8 vs 3.2个月;HR 0.45,95%CI:0.38~0.54,P<0.0001)还是中心评估的PFS(11.0 vs 4.1个月;HR 0.38,95%CI:0.31~0.48,P<0.0001)均有显著获益。
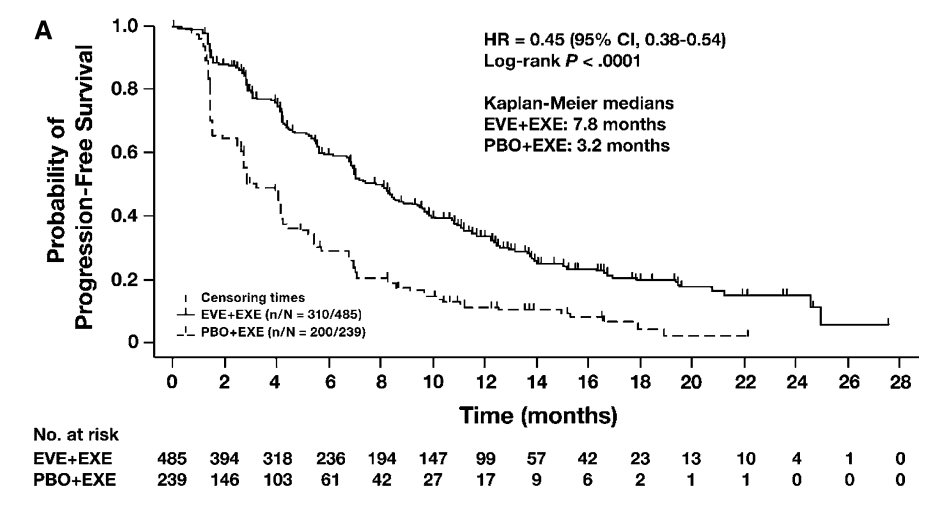
图1. BOLERO-2研究者评估的PFS
国内正在进行的BOLERO-5研究,是一项依维莫司±依西美坦治疗既往来曲唑或阿那曲唑治疗后复发或进展的HR+/HER2-绝经后乳腺癌的2期试验。该研究计划从国内15个中心入组约160例患者,主要终点是研究者评估的PFS,次要终点包括BIRC评估的PFS、OS、ORR、CBR、安全性和耐受性等。目前,研究已接近尾声,从我们中心的部分初步数据来看,依维莫司对中国患者同样有较好的疗效和安全性。相信该研究能够为依维莫司在中国获得乳腺癌适应症提供有力证据。
佟仲生教授:目前,依维莫司在国际上已经获得晚期肾癌、晚期乳腺癌、结节性硬化症等领域的相关适应症;国内已有晚期肾癌等领域的适应症,但在乳腺癌领域已经有不少研究进行验证和探索。比如正在国内进行的BOLERO-5研究(CTR20170589),是一项评估依维莫司联合依西美坦治疗既往来曲唑或阿那曲唑治疗后复发的HR+/HER2-绝经后晚期乳腺癌患者的II期试验,我们中心也有幸参加了该研究,从初步结果来看,依维莫司在中国患者中的疗效和安全性表现也非常不错。
大家对依维莫司其实并不陌生,国际上已经积累很多循证医学证据。例如我们熟知的BOLERO-2研究表明,依维莫司+依西美坦相较于均较依西美坦,无论在研究者评估的PFS,还是中心评估的PFS均有显著获益,OS也看到有临床意义的改善(31.0 vs 26.0个月)。在亚洲人群中,2014年日本学者报道的在BOLERO-2亚洲数据也显示依维莫司+依西美坦带来了4.34个月的PFS延长(8.48 vs 4.14个月;HR 0.62,95% CI:0.41~0.94)。随着国内相关研究的完善,我们期待依维莫司尽快获得乳腺癌适应症,满足更多患者的临床需求。
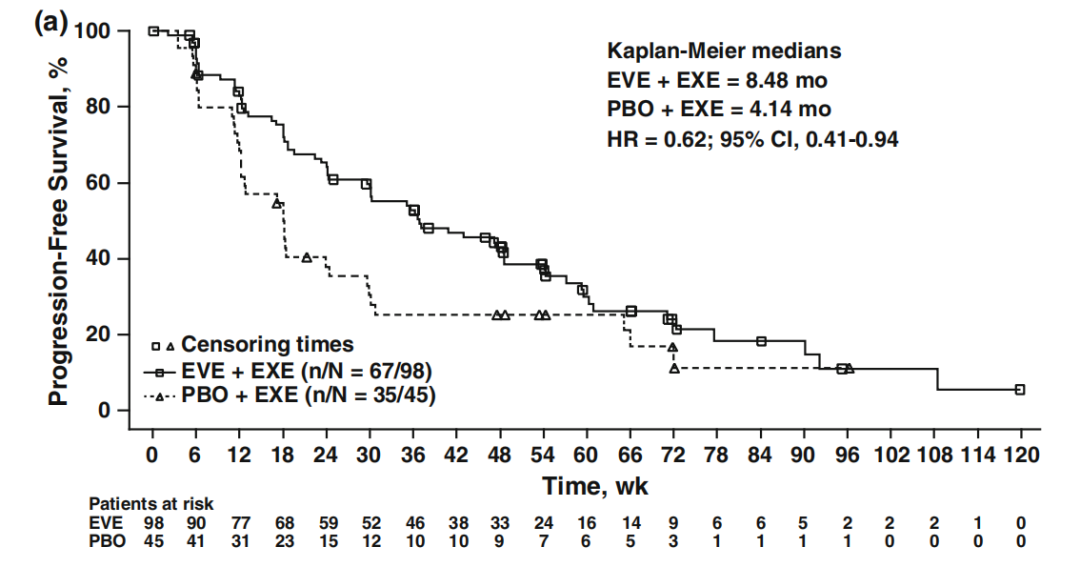
图2.BOLERO-2研究亚洲人群的PFS
王树森教授:正如前所述,基于BOLERO-2研究,依维莫司在国际上获得HR阳性晚期乳腺癌适应症已经有近10年,NCCN等国际指南也推荐依维莫司+内分泌作为二线及后续治疗。从BOLERO-2亚洲人群的数据来看,亚洲患者和总体人群一样有显著的PFS获益。我们也参加了国内的BOLERO-5研究,这项研究与BOLERO-2的设计相似,主要针对AI治疗进展后的绝经后HR+/HER2-患者,目前初步结果来看表现不错。
中国乳腺癌患者有将近60%是绝经前女性。国内已经有报道一项研究者发起的多中心2期MIRACLE研究,该研究则主要针对TAM治疗进展后的绝经前HR+/HER2-患者,共入组199例患者,结果显示相较于来曲唑单药治疗,依维莫司+来曲唑可使PFS显著延长8.2个月(19.2 vs 11.0个月,HR 0.60,95%CI 0.42~0.86;P=0.0053)。从这些国内外已有或正在进行的研究来看,依维莫司在中国HR阳性晚期乳腺癌患者中也同样具有良好的应用前景。
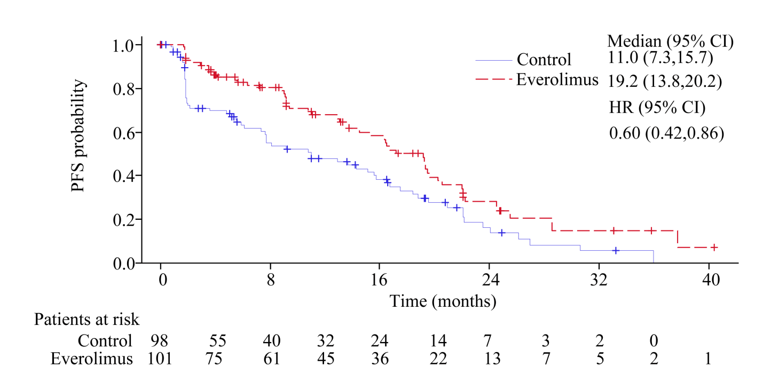
图3. MIRACLE研究ITT人群的PFS
《肿瘤瞭望》:BOLERO-2中既有晚期一线,也有二线,后来的BOLERO-4等研究则探讨了依维莫司一线治疗,以及依维莫司联合不同AI的模式。您如何看待依维莫司在ER阳性晚期乳腺癌中的用药时机及其联合模式?如果mTORi和CDK4/6i均可及,又应该如何选择?
王树森教授:BOLERO-2入组患者均为AI耐药,包括原发(新辅助或辅助治疗12个月内复发)和继发耐药,从亚组分析来看,无论原发(6.83 vs 2.83个月,HR 0.55)还是继发耐药(8.05 vs 3.94个月,HR 0.43)PFS均有改善。因此,依维莫司是可以作为逆转内分泌耐药的选择。当然,BOLERO-2、BOLERO-4研究提示依维莫司作为一线治疗选择也有获益,但是可以更专注于内分泌治疗耐药的人群。
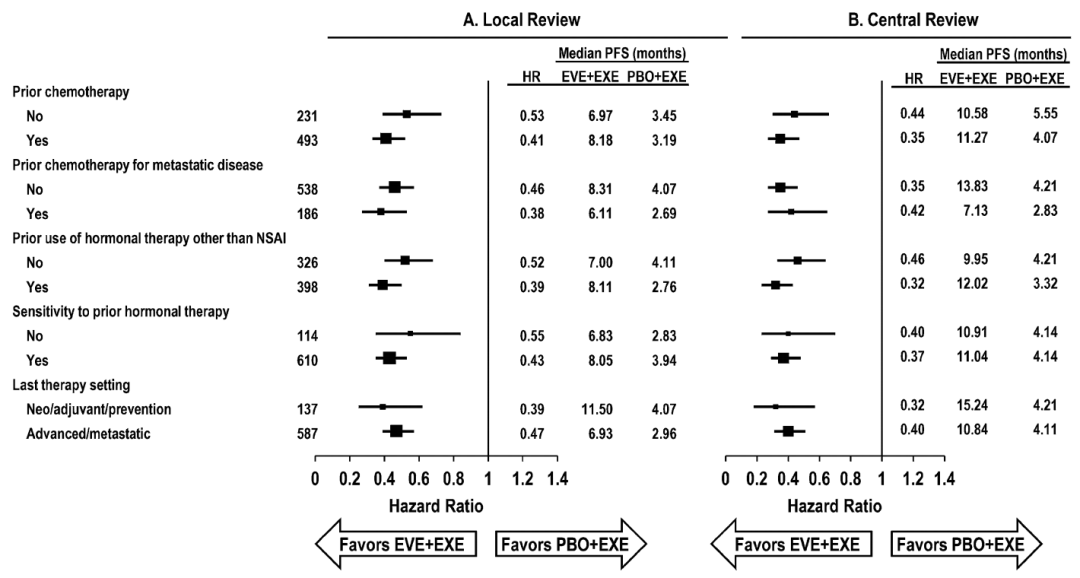
图4. BOLERO-2研究PFS亚组分析
MONALEESA-3研究中51.5%(n=367)为“treatment naïve”(初诊IV,或辅助治疗12个月后复发),属于内分泌敏感人群,其PFS(19.2 vs 33.6个月,HR=0.546)相对于ITT人群(12.8 vs 20.6个月,HR=0.587)获益更明显,而MONALEESA-3研究纳入患者均无AI治疗史,理论上仍属于内分泌敏感人群(或AI敏感人群)。因此,临床中可以将CDK4/6抑制剂向前移,用于内分泌敏感人群的获益更大。
佟仲生教授:mTOR信号通路的活化可引起AIs耐药,对于基因检测明确存在PI3K/AKT/mTOR通路变异的绝经后HR+/HER2-晚期乳腺癌患者的后线治疗可以考虑应用依维莫司。首先,依维莫司可以联合不同内分泌药物,比如TAM治疗进展后的患者可联合来曲唑等AI药物;对于AI进展后的患者,可参考BOLERO-2研究给予依维莫司联合另一类AI,或者像PrE0102研究一样给予依维莫司+氟维司群,后者也比对照组获得了5.2个月的PFS延长(10.3 vs 5.1个月, HR 0.61,95%CI: 0.40~0.92,P=0.02)。
其次,在一线治疗中是否可以选择依维莫司?从现有数据的非头对头比较来看,mTOR抑制剂的PFS获益并没有CDK4/6i明显,后者PFS大多超过2年,MONALEESA-3研究中ribociclib+氟维司群中位PFS甚至达到了33.6个月。因此,目前的临床认识中,依维莫司主要定位在二线治疗,且CDK4/6i对内分泌治疗敏感的人群可能更受益。需要指出的是,关于CDK4/6i进展后使用依维莫司的循证医学证据仍十分有限,这需要将来的临床试验或真实世界研究进行补充。此外,临床中也有相当一部分患者因药物经济性问题而选择单药内分泌治疗,鉴于依维莫司在逆转内分泌耐药的优势,所以此类患者在进展后也可考虑依维莫司。
邵志敏教授:BOLERO-2中有137例为晚期一线治疗,即新辅助或辅助治疗阶段AI治疗失败的患者,结果显示无论是研究者评估的PFS(11.5 vs 4.1个月;HR 0.39,95%CI:0.25~0.624)还是中心评估的PFS(15.2 vs 4.2个月;HR 0.32,95%CI:0.18~0.57)均有显著改善,而且获益程度相较于总体人群更显著。另一项入组202例绝经后HR阳性晚期乳腺癌患者的多中心、单臂、2期BOLERO-4研究,入组患者为内分泌敏感人群(新辅助内分泌停药超过1年,未接受过晚期系统治疗),结果显示依维莫司+来曲唑一线治疗的PFS达到了22.0个月(95%CI:18.1-25.1个月),2年PFS率为42.9%(95%CI:35.0%~50.5%),2年OS率为78.7%(95%CI:72.1%~83.9%)。
可见,依维莫司在一线治疗中也可较单独内分泌治疗增加生存获益,在内分泌治疗敏感人群中,mTORi的PFS获益也接近CDK4/6i,且内分泌耐药也一样获益。对于依维莫司选择什么内分泌药物作为联合,目前MIRACLE、BOLERO-2、PrE0102等研究分别提供了TAM→来曲唑、NSAI→AI、AI→FUL的模式。因此,内分泌治疗仍是HR阳性晚期患者的治疗基石,与依维莫司的联合可根据既往内分泌治疗方案进行替换。
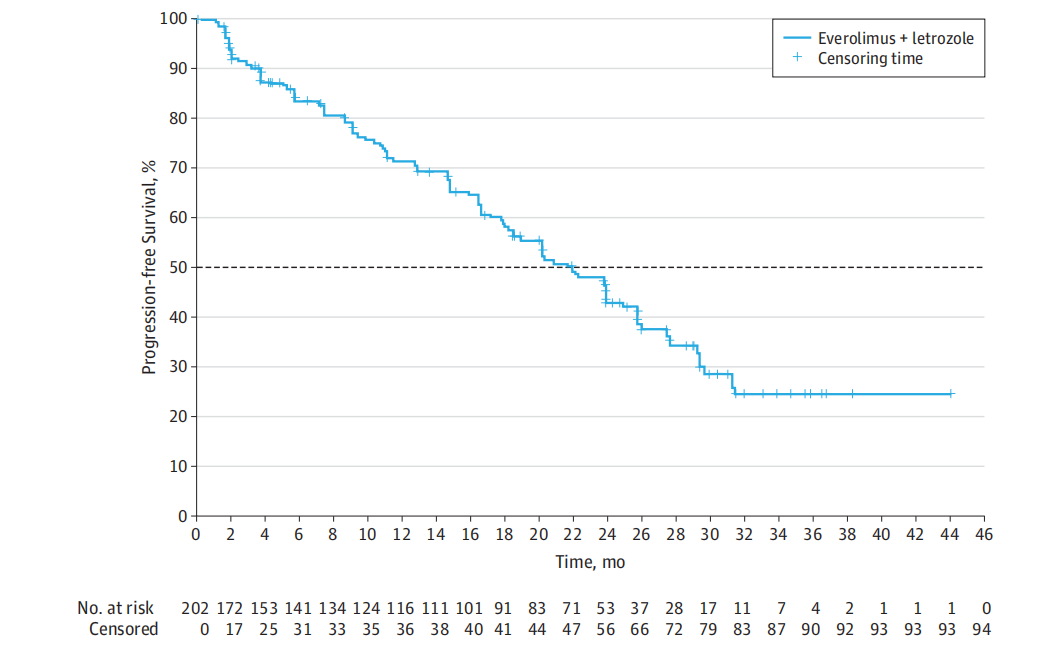
图5. BOLERO-4研究依维莫司一线治疗的PFS生存曲线
《肿瘤瞭望》:国内肿瘤科医生对依维莫司并不陌生,其在肾癌领域已经积累了相当的用药经验。那么,在乳腺癌的治疗中,依维莫司的安全性表现如何,应该注意哪些不良反应的管理?
佟仲生教授:依维莫司的推荐剂量为10 mg,每日1次,常见的不良反应包括口腔黏膜炎、乏力、皮疹、腹泻等,且大多为轻、中度,发生于治疗早期。除了提前告知患者以外,我们也可以采取一些预防或治疗措施,比如预防性使用皮质醇漱口水(SWISH研究:地塞米松0.5 mg/5mL)或淡盐水漱口,可减少口腔黏膜炎的发生;对于出现腹泻症状患者,可以应用洛哌丁胺对症治疗。整体上,患者对依维莫司的耐受性良好,停药率也低于10%,通过积极干预和严密监控可以协助患者完成治疗。
邵志敏教授:在BOLERO-2研究中,与单药组相比,依维莫司常见的明显增加的3-4级不良反应是口腔炎(8% vs 1%),其他研究中也大致相同,但大多发生于治疗早期,随后发生率逐渐下降,且通过减量或暂停可以控制。此外,中国医生在晚期肾癌依维莫司治疗中已经积累了丰富的经验,对晚期乳腺癌的不良事件管理可提供许多借鉴。
《肿瘤瞭望》:中国晚期ER阳性乳腺癌患者仍有巨大的未被满足的临床需求。从现有的循证医学证据来看,您对依维莫司获得国内乳腺癌适应症乃至进入医保有何期待?
邵志敏教授:在HR阳性晚期乳腺癌的治疗中,可将CDK4/6i前推至内分泌敏感的人群;对于内分泌耐药的患者,目前有PI3Ki、mTORi等选择,而依维莫司在国内外已经积累了相当丰富的证据和经验,其获得国内乳腺癌适应症具备良好的条件。希望依维莫司能为中国乳腺癌患者增加新的克服内分泌耐药的方案,并早日进入医保,提高患者的治疗可及性。
佟仲生教授:HR阳性乳腺癌在乳腺癌患者中占比较高,约为60%~70%,且生存期相对较长,在其全程管理中仍有巨大的未被满足的临床需求,尤其是内分泌耐药后的治疗,国内仅有CDK4/6i等有限的选择。依维莫司在国际上已经积累了充分的循证医学证据,国内研究者发起的MIRACLE研究也证实依维莫司可使TAM进展后患者显著获益,而AI进展后的国内BOLERO-5研究也已进入尾声。在肾癌领域,依维莫司也已经有适应症并进入医保,国内肿瘤科医生积累了比较丰富的管理经验,且依维莫司为口服给药,不良反应可耐受,患者依从性很好。因此,我们对依维莫司获得国内乳腺癌适应症乃至进入医保充满信心。
王树森教授:晚期HR阳性乳腺癌仍有巨大的临床需求,尤其是内分泌耐药后的治疗,目前国内CDK4/6抑制剂等靶向药物的选择仍十分有限。国内正在进行的BOLERO-5研究(AI进展后)以及已经报道MIRACLE研究(TAM进展后)将为mTORi依维莫司在中国人群的应用提供循证医学证据。此外,依维莫司在肾癌领域已经进入国家医保,国内医生已经积累了相当充分的依维莫司用药经验,也具备了良好用药基础。希望能尽快推进依维莫司在乳腺癌方面的适应症乃至纳入医保,将提高治疗可及性,造福更多患者。
注:依维莫司尚未在中国取得乳腺癌适应症。本资料目的在于提供疾病领域的相关知识、提高疾病认知水平,非广告用途。本资料中涉及的信息仅供参考,请遵从医生或其他医疗卫生专业人士的意见或指导。
[1]Yardley DA, Noguchi S, Pritchard KI, et al. Everolimus plus exemestane in postmenopausal patients with HR(+) breast cancer: BOLERO-2 final progression-free survival analysis [published correction appears in Adv Ther. 2014 Sep;31(9):1008-9]. Adv Ther. 2013;30(10):870-884.[2]Piccart M, Hortobagyi GN, Campone M, et al. Everolimus plus exemestane for hormone-receptor-positive, human epidermal growth factor receptor-2-negative advanced breast cancer: overall survival results from BOLERO-2†. Ann Oncol. 2014;25(12):2357-2362.[3]Noguchi S, Masuda N, Iwata H, et al. Efficacy of everolimus with exemestane versus exemestane alone in Asian patients with HER2-negative, hormone-receptor-positive breast cancer in BOLERO-2. Breast Cancer. 2014;21(6):703-714.[4]Beck JT, Hortobagyi GN, Campone M, et al. Everolimus plus exemestane as first-line therapy in HR?, HER2? advanced breast cancer in BOLERO-2. Breast Cancer Res Treat. 2014;143(3):459-467.[5]Royce M, Bachelot T, Villanueva C, et al. Everolimus Plus Endocrine Therapy for Postmenopausal Women With Estrogen Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: A Clinical Trial. JAMA Oncol. 2018;4(7):977-984.[6]Rugo HS, Pritchard KI, Gnant M, et al. Incidence and time course of everolimus-related adverse events in postmenopausal women with hormone receptor-positive advanced breast cancer: insights from BOLERO-2. Ann Oncol. 2014;25(4):808-815.[7]http://www.chinadrugtrials.org.cn/clinicaltrials.searchlistdetail.dhtml[8]Kornblum N, Zhao F, Manola J, et al. Randomized Phase II Trial of Fulvestrant Plus Everolimus or Placebo in Postmenopausal Women With Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Metastatic Breast Cancer Resistant to Aromatase Inhibitor Therapy: Results of PrE0102. J Clin Oncol. 2018;36(16):1556-1563.[9]Everolimus in First-line Treatment of Advanced Premenopausal Breast Cancer: Results from MIRACLE (EveroliMus Trial for Advanced PremenopausaL Breast Cancer) Study. SABCS 2019, PD7-08[10]Hortobagyi GN, Stemmer SM, Burris HA, et al. Updated results from MONALEESA-2, a phase III trial of first-line ribociclib plus letrozole versus placebo plus letrozole in hormone receptor-positive, HER2-negative advanced breast cancer [published correction appears in Ann Oncol. 2019 Nov 1;30(11):1842] [published correction appears in Ann Oncol. 2019 Nov;30(11):1842]. Ann Oncol. 2018;29(7):1541-1547.[11]Slamon DJ, Neven P, Chia S, et al. Phase III Randomized Study of Ribociclib and Fulvestrant in Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: MONALEESA-3. J Clin Oncol. 2018;36(24):2465-2472.[12]Tripathy D, Im SA, Colleoni M, et al. Ribociclib plus endocrine therapy for premenopausal women with hormone-receptor-positive, advanced breast cancer (MONALEESA-7): a randomised phase 3 trial. Lancet Oncol. 2018;19(7):904-915.
首批教育部长江学者特聘教授
复旦大学肿瘤研究所所长、乳腺癌研究所所长
复旦大学附属肿瘤医院大外科主任乳腺外科主任
中国抗癌协会乳腺癌专业委员会名誉主委
中华医学会肿瘤学分会副主任委员
上海市抗癌协会乳腺癌专业委员会名誉主任委员
主任医师、硕士研究生导师
中国抗癌协会靶向治疗专业委员会常委
天津市抗癌协会临床化疗专业委员会主委
天津市医药学专家协会肿瘤专业委员会主委
中国乳腺癌专业委员会委员
天津医学会肿瘤学分会委员
《中国肿瘤临床》杂志编委
《天津医药》编委
《中华乳腺病杂志》编委
《中国综合临床》编委
主任医师、教授、医学博士、博士生导师
中山大学肿瘤防治中心
乳腺癌内科首席专家、内科乳腺病区主任
中国研究型医院协会乳腺癌专业委员会副主任委员
中国抗癌协会乳腺癌专业委员会常务委员
中国临床肿瘤协会乳腺癌专业委员会常务委员
中国抗癌协会肿瘤临床化疗专业委员会青委会副主任委员
国家肿瘤质控中心乳腺癌质控专业委员会委员
中国乳腺癌筛查与早诊早治指南专家委员会委员





 京公网安备 11010502033352号
京公网安备 11010502033352号